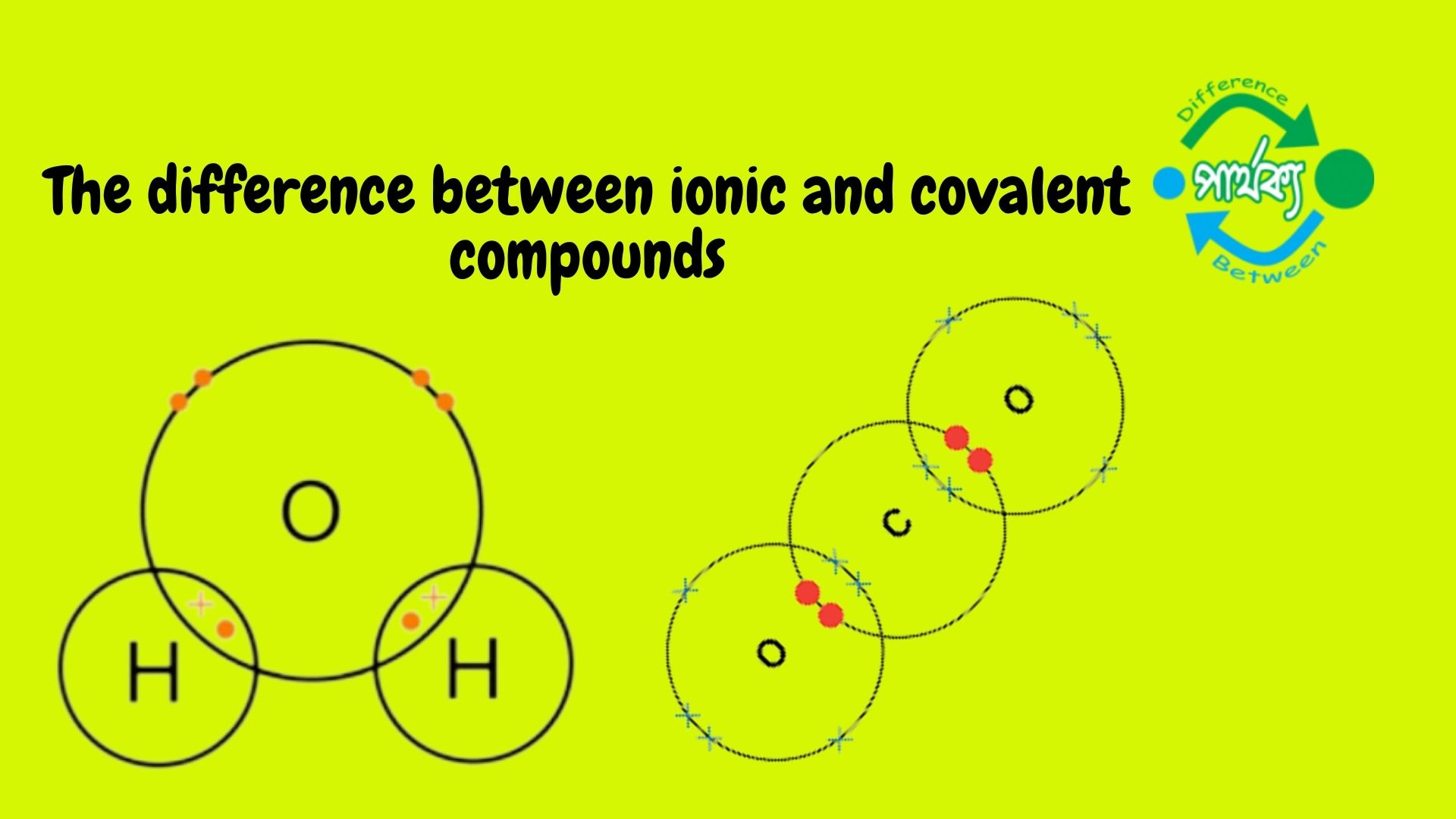
আয়নিক যৌগ (Ionic compound):
ইলেকট্রন বর্জন ও গ্রহন করে বিপরীত চার্জযুক্ত আয়ন সৃষ্টির মাধ্যমে পরস্পরের মধ্য স্থির বৈদ্যুতিক আকর্ষণের ফলে দুটি পরমাণুর মধ্যে আয়নিক বন্ধন সৃষ্টির মাধ্যমে যে যৌগের সৃষ্টি হয় তাকে আয়নিক যৌগ বলে। রসায়নে,আয়নিক যৌগ হচ্ছে একটি রাসায়নিক যৌগ যা আয়নগুলোর মধ্যে তড়িৎবলের মাধ্যমে যুক্ত থাকে।
যৌগটি অবশ্য নিরপেক্ষ কিন্তু যা গঠিত হয় ধনাত্মক চার্জ যাকে বলা হয় ক্যাটায়ন এবং ঋণাত্মক চার্জ যাকে বলা হয় অ্যানায়ন। এগুলো সাধারন আয়ন হতে পারে যেমন সোডিয়াম ক্লোরাইড এ থাকে সোডিয়ান আয়ন (Na+) এবং ক্লোরিন আয়ন (Cl-) অথবা বহুআণবিক প্রজাতি যেমন অ্যামোনিয়াম কার্বনেট এ অ্যামোনিয়াম (NH4+) এবং থাকে কার্বনেট আয়ন(CO3^2-)।
আয়নিক যৌগের আলাদা আলাদা আয়ন থাকতে পারে যাদের একাধিক নিকটাত্মীয় প্রতেবেশি থাকতে পারে যারা পরমাণুর অংশ না হয়ে বরং ত্রিমাত্রিক কেলাসে ধারাবাহিক ভাবে তিনমাত্রিক গঠনের জাল হিসেবে থাকে।
যেসব আয়নিক যৌগে হাইড্রোজেন আয়ন (H+)থাকে তাদের এসিড হিসেবে এবং যারা হাইড্রোক্সিল আয়ন (OH-) বা অক্সাইড (O2-) হিসেবে থাকে তাদের ক্ষার হিসেবে শ্রেণিবিন্যাস করা হয়। যেসব আয়নিক যৌগে এসব থাকে না তাদের লবন বলা হয় যা এসিড ক্ষার বিক্রিয়ায় উৎপন্ন হতে পারে। উদাহরন – NaCl, CaO, MgCl2.
সমযোজী যৌগ (covalent compound):
নিকটতম নিস্ক্রিয় গ্যাসের ন্যায় সুস্থিত ইলেকট্রন বিন্যাস লাভের চেষ্টায় একই বা ভিন্ন মৌলের পরমাণুগুলি তাদের সর্ববহিস্থ কক্ষের এক বা একাধিক ইলেকট্রন জোড় সমভাবে ব্যবহারের মাধ্যমে পরমাণু গুলির যুক্ত হওয়ার ক্ষমতাকে সমযোজ্যতা বলে । এইভাবে গঠিত যৌগকে সমযোজী যৌগ বলে ।
প্রধানত সমযোজী যৌগের বাঁধাই গঠনের, সমযোজী যৌগের বলা এবং গঠন একত্রিত অ ধাতব উপাদানের বিভিন্ন ধরণের অধিকাংশ জৈব পরমাণু যেমন CO2, ClO2, B2H6, BF3, NCl3, ইত্যাদি। যৌগ সব যৌগিক সমযোজী অন্তর্গত। সমযোজী যৌগের সাধারণত একটি পৃথক অণু আছে। বিন্দু যৌগ সাধারণত সমযোজী হয় গলন, নিম্ন ফুটন্ত পানিতে অদ্রবণীয়, অ পরিবাহী গলিত রাষ্ট্র, কম কঠোরতা কিছু আয়নের যৌগিক এছাড়াও covalently আবদ্ধ অস্তিত্ব নাও থাকতে পারে।
যেমন- NaOH অণু উভয় আয়নের বন্ড সমযোজী বন্ধন আছে। সসীম অণুতে covalently থেকে জোড়া হয়, এবং অণুর মধ্যে Van Der Waals বাহিনী কর্ম দ্বারা একটি স্বচ্ছ মধ্যে, এটা যেমন ক্রিস্টাল থেকে CO2, বেনজিন স্ফটিক হিসেবে আণবিক স্ফটিক, আদর্শ ঘনীভূত। আনলিমিটেড ক্রিস্টাল অণু যেমন একটি ডায়মন্ড ক্রিস্টাল, একক স্ফটিক সিলিকন, এবং সাদা সিলিকা।
আয়নিক ও সমযোজী যৌগের মধ্যে পার্থক্যঃ
আয়নিক যৌগের আলাদা আলাদা আয়ন থাকতে পারে যাদের একাধিক নিকটাত্মীয় প্রতেবেশি থাকতে পারে। আয়নিক ও সমযোজী যৌগের মধ্যে পার্থক্য নিম্নরুপঃ
১। ইলেকট্রন বর্জন ও গ্রহন করে বিপরীত চার্জযুক্ত আয়ন সৃষ্টির মাধ্যমে পরস্পরের মধ্য স্থির বৈদ্যুতিক আকর্ষণের ফলে দুটি পরমাণুর মধ্যে আয়নিক বন্ধন সৃষ্টির মাধ্যমে যে যৌগের সৃষ্টি হয় তাকে আয়নিক যৌগ বলে। অন্যদিকে একাধিক ইলেকট্রন জোড় সমভাবে ব্যবহারের মাধ্যমে পরমাণু গুলির যুক্ত হওয়ার ক্ষমতাকে সমযোজ্যতা বলে । এইভাবে গঠিত যৌগকে সমযোজী যৌগ বলে।
২। ধাতু ও অধাতুর মধ্যে আয়নিক যৌগ গঠিত হয়। অন্যদিকে অধাতু-অধাতু সমযোজী যৌগ গঠন করে।
৩। আয়নিক যৌগ গঠনের ক্ষেত্রে ইলেকট্রন আদান প্রদান ঘটে। অন্যদিকে সমযোজী যৌগ গঠনের ক্ষেত্রে ইলেকট্রন শেয়ার ঘটে।
৪। আয়নিক যৌগের গলনাঙ্ক ও স্ফুটনাঙ্ক বেশি। অন্যদিকে সমযোজী যৌগের গলনাংক ও স্ফুটনাংক কম হয়।
৫। আয়নিক যৌগ সমূহ পানিতে দ্রবণীয়। অন্যদিকে সমযোজী যৌগ পানিতে অদ্রবণীয়।
৬। আয়নিক যৌগ গলিত বা দ্রবীভূত অবস্থায় বিদ্যুৎ পরিবহন করে। অন্যদিকে সমযোজী যৌগ সমূহ বিদ্যুৎ পরিবহন করে না।
৭। আয়নিক যৌগ সমূহ কেলাস গঠন করতে পারে। অন্যদিকে সমযোজী যৌগ সমূহ সাধারণত তরল বা গ্যাসীয় অবস্থায় থাকে।
রসায়ন সংক্রান্ত আরো পার্থক্য পড়ুনঃ Chemistry
আরোও পার্থক্য পড়ুনঃ যোগান রেখা ও সূচির মধ্যে পার্থক্য, স্বাধীন চলক ও অধীন চলকের মধ্যে পার্থক্য, একমাত্রিক ও দ্বিঘাত অপেক্ষকের মধ্যে পার্থক্য, মুদ্রাস্ফীতি এবং অপসারণের মধ্যে পার্থক্য, সংকীর্ণ মুদ্রা ও বিস্তৃত মুদ্রার মধ্যে পার্থক্য, মোট, গড় ও প্রান্তিক ব্যয়ের মধ্যে পার্থক্য, স্বল্পকালীন ও দীর্ঘকালীন উৎপাদন ব্যয়ের মধ্যে পার্থক্য, দামের স্থিতিস্থাপকতা এবং চাহিদার আয়ের স্থিতিস্থাপকতার মধ্যে পার্থক্য