মোলারিটি (Molarity):
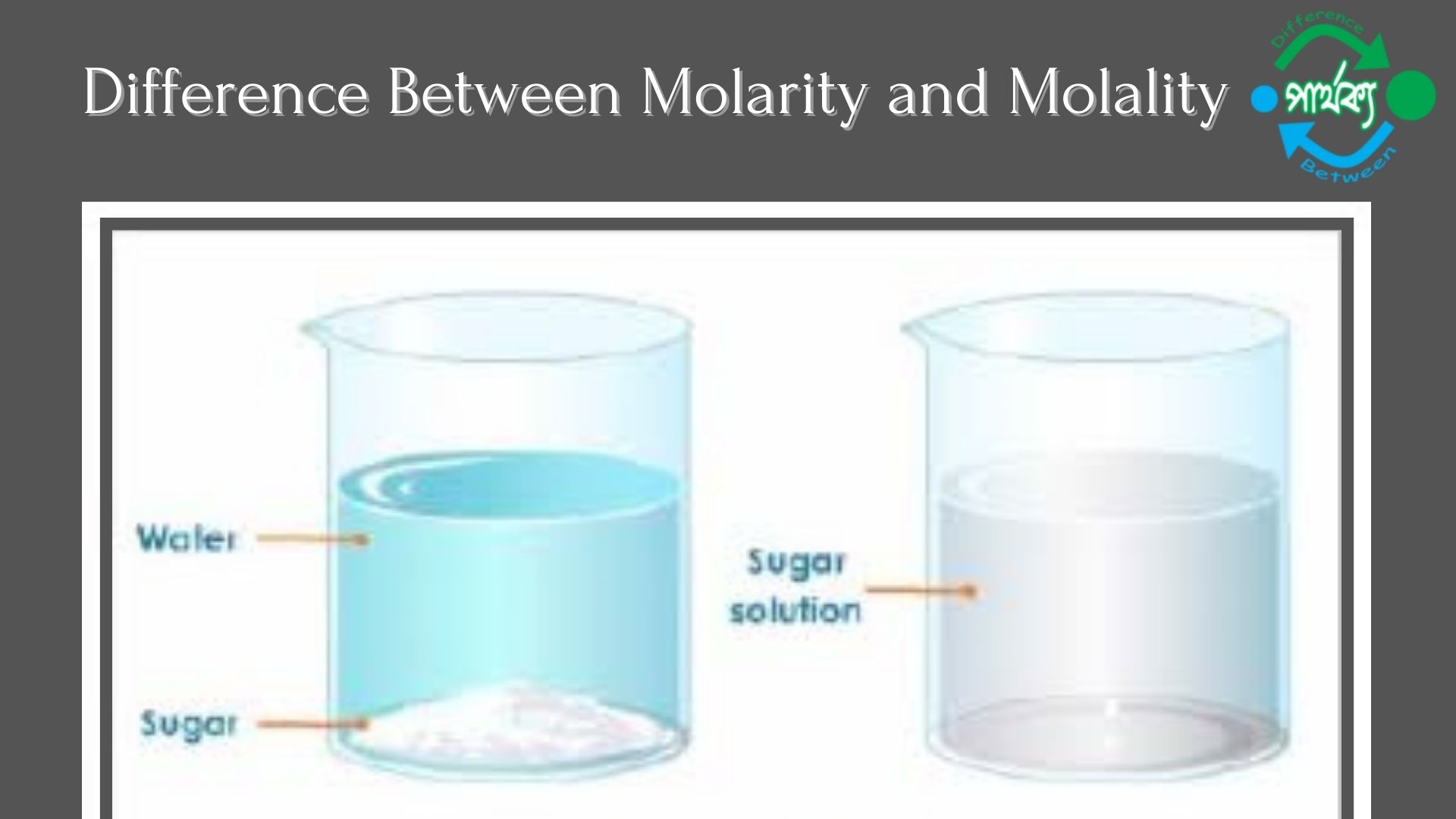
কোনো নির্দিষ্ট তাপমাত্রায় ১ লিটার দ্রবণের মধ্যে দ্রবীভূত দ্রবের মোল সংখ্যাকে দ্রবণের মোলারিটি বলে। মোলারিটিকে M দ্বারা প্রকাশ করা হয়।
যেমনঃ ১ মোল NaCl= 58.5g। একটি নির্দিষ্ট তাপমাত্রায় ১ লিটার দ্রবণের মধ্যে যদি এক মোল Nacl বা 58.5g NaCl। দ্রবীভূত থাকে তবে ঐ দ্রবণকে NaCl এর মোলার দ্রবণ বলে এবং দ্রবণটির মোলারিটি হচ্ছে ১।
মোলালিটি (Molality):
কোন দ্রবণের প্রতি এক কিলোগ্রাম দ্রাবকে দ্রবীভূত দ্রবের মোলসংখ্যা বা গ্রাম আণবিক ভরসংখ্যাকে ঐ দ্রবণে দ্রবের মোলালিটি বলে। অর্থাৎ কোন দ্রবণের প্রতি এক কিলোগ্রাম দ্রাবকে দ্রবীভূত দ্রবের মোলসংখ্যা আণবিক ভর সংখ্যাকে ঐ দ্রবণে দ্রবের মোলালিটি বলে। মোলালিটি দ্রাবকের ওজন এবং দ্রবের মোল সংখ্যার সাথে সম্পর্কিত। তাপমাত্রার পরিবর্তনে দ্রাবকের ওজন এবং দ্রবের মোল সংখ্যার কোন পরিবর্তন হয় না। তাই দ্রবণের মোলালিটি তাপমাত্রার উপর নির্ভরশীল নয়।
Molality হল দ্রাবক প্রতি একক দ্রাবক ময়দার তাল । এটি গুরুত্বপূর্ণ দ্রাবক ভর ভর ব্যবহৃত হয় না এবং সমাধান ভর না। মৌল ঘনত্ব সঙ্গে লেবেল সমাধানগুলি একটি নিম্ন ক্ষেত্রে মি সঙ্গে চিহ্নিত করা হয়। একটি 1.0 মি দ্রবণটি প্রতি একক দ্রাবক প্রতি একক দ্রাবক রয়েছে।
মোলারিটি ও মোলালিটির মধ্যে পার্থক্যঃ
মোলারিটি ও মোলালিটির মধ্যে অনেক বৈশিষ্ট্যগত পার্থক্য রয়েছে। তাই নিচে মোলারিটি ও মোলালিটির মধ্যে পার্থক্য দেখানো হয়েছে-
১। কোনো নির্দিষ্ট তাপমাত্রায় ১ লিটার দ্রবণের মধ্যে দ্রবীভূত দ্রবের মোল সংখ্যাকে দ্রবণের মোলারিটি বলে। অন্যদিকে, কোন দ্রবণের প্রতি এক কিলোগ্রাম দ্রাবকে দ্রবীভূত দ্রবের মোলসংখ্যা বা গ্রাম আণবিক ভরসংখ্যাকে ঐ দ্রবণে দ্রবের মোলালিটি বলে।
২। মোলারিটি মূলত দ্রবণের আয়তন এবং দ্রবের মোল সংখ্যার সাথে সম্পর্কিত। সাধারণত তাপমাত্রার পরিবর্তনে দ্রবের মোল সংখ্যার কোন পরিবর্তন না হলেও দ্রবণের আয়তনের পরিবর্তন হয়ে থাকে, তাই দ্রবণের মোলারিটি তাপমাত্রার উপর নির্ভরশীল।
অন্যদিকে, মোলালিটি দ্রাবকের ওজন এবং দ্রবের মোল সংখ্যার সাথে সম্পর্কিত। তাপমাত্রার পরিবর্তনে দ্রাবকের ওজন এবং দ্রবের মোল সংখ্যার কোন পরিবর্তন হয় না। তাই দ্রবণের মোলালিটি তাপমাত্রার উপর নির্ভরশীল নয়।
৩। মোলারিটি দ্রবণের আয়তনের ওপর নির্ভরশীল। অন্যদিকে, মোলালিটি দ্রাবকের ভরের ওপর নির্ভরশীল।
৪। মোলারিটি তাপমাত্রার ওপর নির্ভরশীল। অন্যদিকে, মোলালিটি তাপমাত্রার ওপর নির্ভরশীল নয়।