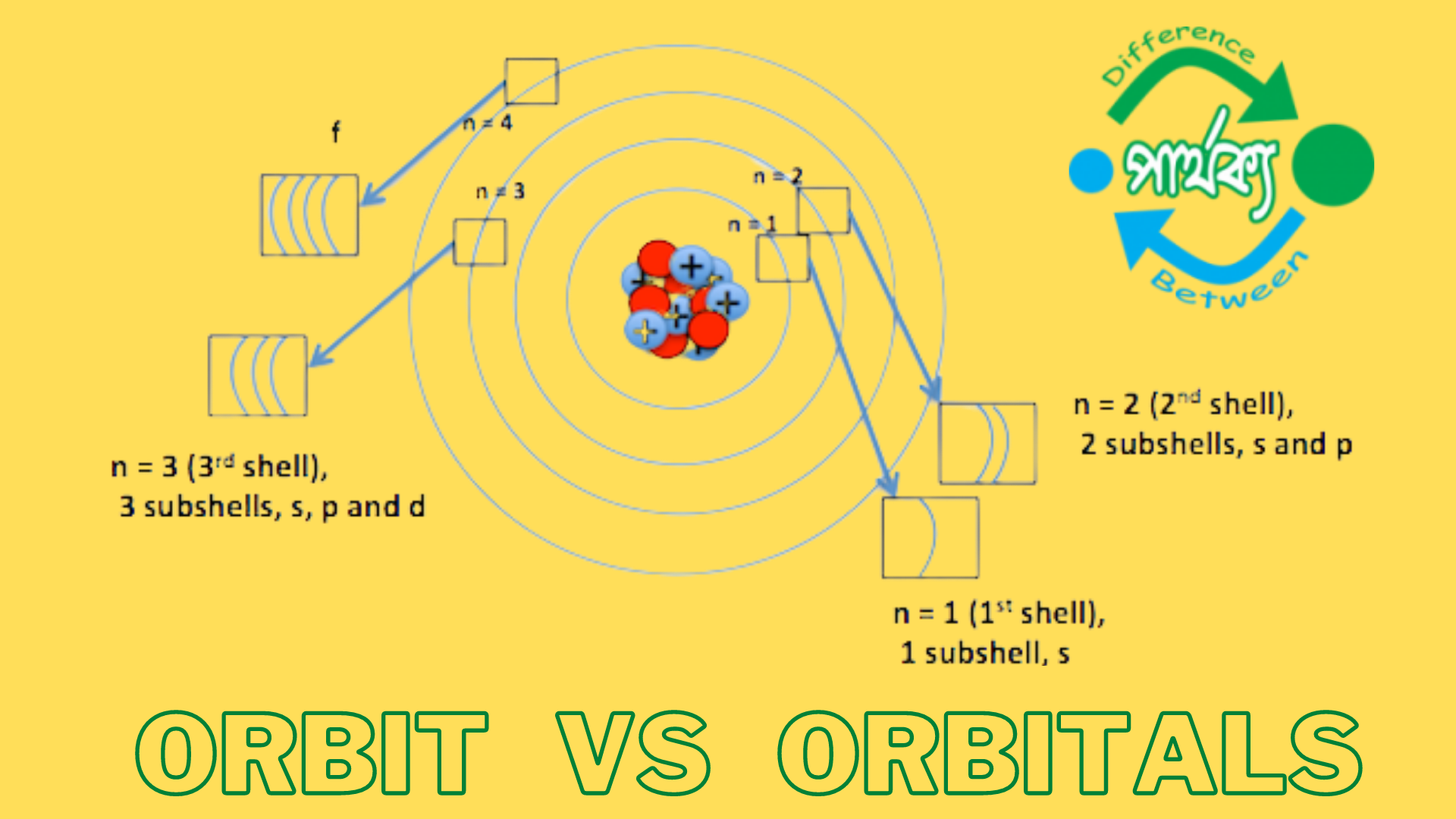
অরবিট(Orbit)ঃ
পরমাণুতে নিউক্লিয়াসের চতুর্দিকে ইলেকট্রন আবর্তনের জন্য কতগুলো নির্দিষ্ট শক্তি বিশিষ্ট কক্ষপথ রয়েছে। এদের প্রধান শক্তিস্তর বা শেল বলে। এই প্রধান শক্তি স্তরই অরবিট নামে পরিচিত।
অরবিটাল(Orbital)ঃ
নিউক্লিয়াসের চারদিকে যে নির্দিষ্ট ত্রিমাত্রিক স্থানে কোন নির্দিষ্ট শক্তিস্তরে ইলেকট্রনের অবস্থানের সম্ভাবনা বেশি থাকে তাকে অরবিটাল বলে। অর্থাৎ নিউক্লিয়াসের চতুর্দিকে ইলেকট্রনের আবর্তনের সর্বাধিক সম্ভাব্য অঞ্চলকে অরবিটাল বলে।
অরবিট ও অরবিটাল এর মধ্যে পার্থক্যঃ
১। অরবিট নিউক্লিয়াসের চারিদিকে সামতলিকভাবে অথবা দ্বি-মাত্রিকভাবে অবস্থান করে। এর ইলেকট্রন-ধারণ সংখ্যা 2n2 , যেখানে n = কক্ষপথের ক্রমিক সংখ্যা। নিউক্লিয়াসের ধনাত্মক এনার্জি এবং ইলেকট্রনের ঋণাত্মক এনার্জির পারস্পরিক ক্রিয়ার ফলে সচল ইলেকট্রনের কৌণিক ভরবেগ আবর্তনকালে সর্বদা একই থাকে, ফলে কক্ষপথের সৃষ্টি হয়। অন্যদিকে, অরবিটাল হল পরমাণুর অন্তঃস্থ এমন একটি অনির্দিষ্ট স্থান বা অঞ্চল যেখানে ইলেকট্রন পাওয়ার সম্ভাবনা সবচেয়ে বেশী। হাইজেনবার্গের অনিশ্চয়তা সূত্র থেকে আমরা বুঝতে পারি যে একটি নির্দিষ্ট মুহূর্তে ইলেকট্রনের গতিবেগ ও অবস্থান একসঙ্গে বলা সম্ভব নয়, তাই এমন একটি অনির্দিষ্ট স্থান নির্বাচন করা হয়, যেখানে কোন এক মুহূর্তে ইলেকট্রন পাওয়ার সম্ভাবনা সবথেকে বেশী, আর তাকেই অরবিটাল বলা হয়। অরবিটাল বাস্তবে পরমাণুর মধ্যে, তথা নিউক্লিয়াসের চারদিকের ত্রিমাত্রিক স্থানকে নির্দেশ করে।
২। প্রধান শক্তিস্বর বা প্রধান কোয়ান্টাম সংখ্যাই অরবিট। অন্যদিকে উপস্তরের সম্ভাব্য অঞ্চলটাই অরবিটাল ।
৩। অরবিটকে K,L,M,N,O ইত্যাদি দ্বারা প্রকাশ করা হয়। অন্যদিকে অরবিটালকে S, Px, PY ,PZ ইত্যাদি দ্বারা প্রকাশ করা হয়।
৪। একটি অরবিটে সর্বাধিক 2n2 ইলেকট্রন থাকতে পারে। অন্যদিকে একটি অরবিটালে সর্বাধিক 2টি ইলেকট্রন থাকতে পারে।
৫। অরবিট হলো নির্দিষ্ট কক্ষপথ যাকে কেন্দ্র করে ইলেক্ট্রন ঘুরে। অন্যদিকে অরবিটাল হলো নিউক্লিয়াসের চারদিকের এমন একটি স্থান যেখানে ইলেক্ট্রনের আধিক্য বেশি।